Diabéteszes betegek kardiovaszkuláris terápiája gyakorlati tapasztalatok alapján
Közismert, hogy a cukorbetegség (diabetes mellitus) – elsősorban az ún. jóléti társadalmakban – nagyon sok embert érint. 2014-ben az OEP-adatbázisban szereplő 2-es típusú cukorbetegek száma 727 000 volt, amely a teljes lakosságra vonatkoztatva 7,3%-os előfordulást jelent. A standardizált prevalencia közel másfél évtized alatt 4,2%-ról 6,4%-ra nőtt. 2017 novemberében – a statisztikai adatok szerint – Magyarországon közel 1 millió ember volt diabéteszes. Ennek kb. 90%-a 2-es típusú.
Azt is régóta tudjuk, hogy a diabétesz súlyos szív- és érrendszeri szövődmények kialakulásához vezet. Egyaránt károsodhatnak a nagy és az egészen kicsi artériák is. Ezt nevezzük makro- és mikrovaszkuláris károsodásnak. Nagyon súlyos következményei lehetnek az agyat, a szívet és az alsó végtagokat ellátó artériák érelmeszesedésének (agyér-elmeszesedés, koszorúér-elmeszesedés, alsóvégtagi érszűkület), s az ez által kialakuló akut vagy krónikus keringési zavarnak. Ilyen mechanizmusú kórfolyamatok következménye lehet a stroke, a szív esetében a miokardiális infarktus, illetve az angina pectoris. Az alsóvégtagi artériák atheroscleroticus szűkületei pedig gyengeséghez, járászavarhoz, súlyosabb esetekben pedig fekélyképződéshez, szövetelhaláshoz vezethetnek. A mikrovaszkuláris „érintettség” a szem belső struktúrájának károsodását (retinopathia), a vese funkcióinak beszűkülését (nephropathia), illetve a perifériás idegek megbetegedését (neuropathia) okozhatja. Ezeknek a szövődményeknek a kialakulását, szerencsés esetben, el lehet kerülni, a szervi működészavarokhoz vezető kórfolyamatokat le lehet lassítani abban az esetben, ha a betegek szénhidrátháztartásának zavarát megfelelő időben kezdjük kezelni. A gyakorlat azonban azt mutatja, hogy a cukorbetegség diagnózisának felállításakor az esetek jelentős részében már a makrovaszkuláris szövődmények is kimutathatók. Éppen ezért nagyon fontos a diabéteszes kórállapot fennállásának mielőbbi felismerése, és az antidiabetikus kezelés megkezdése.
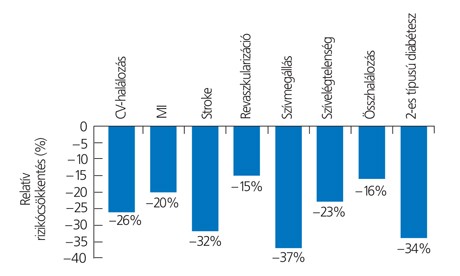
Az érrendszeri szövődmények kialakulásának elkerülése érdekében alapvető a szénhidrátháztartás rendezése. Ezt a megfelelő diéta betartásával, az addigi életmód némely elemének korrekciójával (gyakoribb és intenzívebb testmozgás, testsúlycsökkentés stb.), illetve korszerű antidiabetikus terápia bevezetésével lehet biztosítani. Mindezek mellett azonban vannak olyan készítmények, amelyek az antidiabetikus terápiától függetlenül a szív- és érrendszer károsodásával szemben védelmet biztosítanak (kardiovaszkuláris protektív hatás). Ezek között elsőként említendők a renin–angiotenzin–aldoszteron-rendszer (RAAS) aktivitásának gátlói. A fokozott RAAS-aktiváció ugyanis a vér, illetve a szöveti angiotenzin-II-koncentráció emelkedéséhez vezet. Az angiotenzin-II pedig magas dózisban számos kedvezőtlen hatással bír. Erős érösszehúzó hatású, amely vérnyomás-emelkedést és a szívre háruló terhelés jelentős növekedését eredményezi. Az angiotenzin-II magas szintje az aldoszteronkoncentrációt is növeli. Ennek következtében a veséken keresztül kevesebb víz és nátrium ürül, a vérnyomás ezáltal is emelkedik. Mindezek mellett a hiperaldoszteronizmus a kardiovaszkuláris rendszerben fokozza a kóros kötőszövet-képződést (kardiovaszkuláris remodelláció). A fokozott RAAS-aktivitás mellett számos további kedvezőtlen hatással is számolhatunk. Növekedési faktorok aktiválódnak, kóros szívizom-hipertrófia jön létre, fokozódik a trombózishajlam, a szívizomsejtek száma az intenzívebb nekrotikus és/vagy apoptotikus folyamatok által érdemben csökken, továbbá a megváltozott intracelluláris folyamatok következtében a myocyták kontrakciója károsodik. Az angiotenzin konvertáló enzim gátlásával (ACE-gátlás) visszafogható/csökkenthető az angiotenzin-II képződése. Értelemszerűen az angiotenzin-II által kiváltott kedvezőtlen hatások is vagy jóval enyhébben vagy egyáltalán nem jelentkeznek. Nagyon fontos hangsúlyozni, hogy az ACE-gátlók kiváltotta kedvező hatások vérnyomáscsökkentő hatásuktól függetlenül is megjelennek. Ennek egyértelmű bizonyítékát szolgáltatták a ramiprillal folytatott HOPE- (1), MICRO-HOPE- (2) és a HOPE-TOO-, valamint a perindoprillal végzett EUROPA-vizsgálatok eredményei (1. ábra).
Az ACE-gátlók ugyanis érbetegek, illetve nagy kardiovaszkuláris rizikójú egyének körében csökkentik a major szív- és érrendszeri megbetegedések kialakulásának esélyét (HOPE, EUROPA), javítják a diabéteszes betegek életkilátásait (MICRO-HOPE), illetve kedvezően befolyásolják, lelassítják az érelmeszesedési folyamatokat (SECURE) (3).
A szív- és érrendszeri megbetegedésekben és/vagy hipertóniában szenvedők kezelése során gyakran alkalmazunk dihidropiridin típusú (DHP) kálciumcsatorna-blokkoló gyógyszereket (Ca-antagonisták). Az elmúlt évtizedek vizsgálatai rávilágítottak arra, hogy ezek a készítmények nemcsak kiváló vérnyomáscsökkentők, hanem számos további kedvező tulajdonsággal is rendelkeznek. Így pl. csökkentik a trombocitaaggregációt, antioxidáns hatással bírnak, gátolják a glomeruláris sejtproliferációt, elősegítik a diurézist, s mindezek mellett metabolikusan semlegesek. Kimutatható volt továbbá az, hogy az artériák falában zajló, érelmeszesedéshez vezető kórfolyamatok lassítására/gátlására is képesek. Fokozzák az értágulatot okozó nitrogén-monoxid termelődését, gátolják a simaizomsejt-proliferációt és -migrációt, lassítják a lipidoxidációt, továbbá egyfajta endothelsejt-védelmet is biztosítanak. Mindezeknek eredményeképpen lassul az ateroszklerotikus folyamat progressziója. Ezt bizonyítani lehetett intravaszkuláris UH-vizsgálattal (CAMELOT-study), továbbá a PREVENT-tanulmány (4) eredményeivel, amelyek rámutattak arra, hogy az amlodipinnel kezelt betegek csoportjában kisebb gyakorisággal fordultak elő a szív- és érrendszeri megbetegedések, illetve ritkábban volt szükség a koszorúerek műtéti vagy katéteres úton történő kezelésére.
Az ACE-gátlók és a Ca-antagonisták együttadásának eredményességét bizonyította a két, nagy esetszámú, hazai betegpopulációt érintő RAMONA- és RAMSES-vizsgálat is, amelyekben részben hipertóniás, részben hipertóniás és metabolikus szindrómában szenvedő betegeket ACE-gátló (ramipril) és Ca-antagonista (amlodipin) fix kombinácós terápiában részesítettek. A négy, illetve a hat hónapos kezelés során mind a rendelői, mind az ABPM-eredmények szignifikáns és hatékony vérnyomáscsökkenést bizonyítottak.
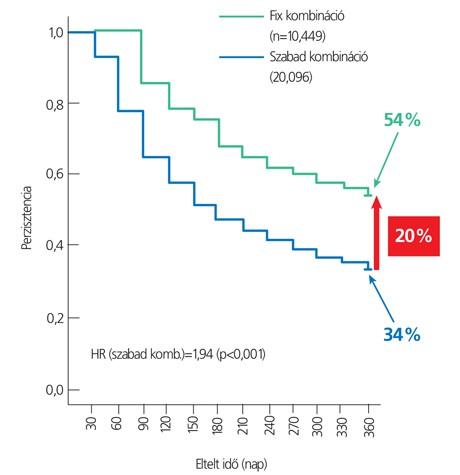
A RAMONA-vizsgálatban (5) a betegek 52%-a, a RAMSES-tanulmányban (6) 75%-uk elérte a célvérnyomás-értéket a ramipril/ amlodipin FDC (fix dózisú kombináció) segítségével (2. ábra). A vizsgálat kapcsán nyert adatok azt is alátámasztották, hogy a hatóanyagok a metabolikus (szénhidrát- és lipidháztartást jellemző) paramétereket tendenciaszerűen kedvező irányba változtatták. Mindezek mellett ezek a vizsgálatok arra is rávilágítottak, hogy a gyógyszerszedési hűség lényegesen nagyobb az ún. fix kombinációk alkalmazása mellett. Nem véletlen, hogy a hazai és a nemzetközi szakmai grémiumok is ezt javasolják. A legfrissebb európai hipertóniaajánlás (ESC/ESH – 2018) egyértelműen leszögezi, hogy a hipertóniás betegek legtöbbjénél a kezelést fix kombinációval kell kezdeni (8).
Nagyon sok olyan diabéteszes beteg van, akinek a társ- vagy kísérőbetegségét, esetlegesen a már kialakult szövődményeket béta-blokkolóval és/vagy diuretikummal lehet/kell kezelni. Ilyen esetekben egyáltalán nem mindegy, hogy az alkalmazott szerek hogyan befolyásolják a beteg szénhidrátháztartását.
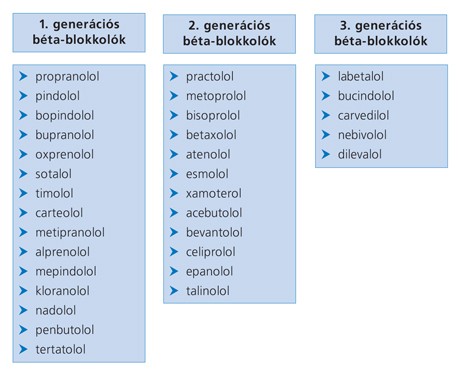
A béta-blokkolókat 3 generációba soroljuk. Az 1. generációs béta-blokkolók a nem béta-1-szelektív szerek, a 2. generációsok elsősorban a béta-1-receptorokat blokkolják, míg a 3. generáció szereit értágító képességük (vazodilatátorok) alapján sorolták egy csoportba (3. ábra).
Tudni kell azonban azt, hogy a béta-blokkolók számos egyéb – a terápiás hatékonyságukat befolyásoló – képességgel is rendelkeznek, s ezekben jelentős különbségeket mutatnak. Így például eltérő a béta-1-szelektivításuk mértéke, hatáserősségük, hatástartamuk, intrinszik szimpatomimetikus aktivitásuk, inzulinrezisztenciára kifejtett képességük, inverz agonista aktivitásuk stb. (1. táblázat). Továbbá vannak antiapoptotikus, antioxidáns, antiproliferatív hatással bíró, víz- vagy zsíroldékony készítmények.
Emellett azt sem szabad elfelejteni, hogy béta-receptorok nemcsak a szívben és az érrendszerben, hanem számos szervben és szervrendszerben is megtalálhatók. Ennek megfelelően a béta-receptorok ingerlése, illetve blokkolása – szelektíven vagy nem szelektíven ható, esetlegesen alfareceptor-blokkoló tulajdonsággal is rendelkező – béta-blokkolóval a szervezet egésze részéről egy összetett választ generál. Mindezt tudva már érthető, hogy két, a 2. generációhoz tartozó béta-blokkoló adásával kiváltott szervezeti reakcióban, s ezáltal a készítmények terápiás eredményességében óriási különbségek lehetnek. A béta-blokkolók hatásaiban meglévő különbségek már a klinikumban használt paraméterek megváltoztatásában – azoknak irányában és/vagy mértékében – is megjelenhetnek. Pl. az emberi szervezet szénhidrát- és/vagy lipidháztartását is eltérően (eltérő irányban vagy mértékben) befolyásolják. Összességében elmondható, hogy míg metabolikus hatásaikat tekintve a 2. generációs béta-blokkolók a szénhidrát- és lipidháztartást jellemző paramétereket kedvezőtlen irányban változtatják meg, addig a 3. generációs készítmények az anyagcserére kifejtett hatásaikat tekintve inkább semlegesnek mondhatók. Ezzel némileg összefüggésben vizsgálatok bizonyították, hogy a 2. generációs béta-blokkolók szedése a cukorbetegség kialakulását elősegíti (7).
Tekintettel arra, hogy nincs két – minden tulajdonságában – azonos béta-blokkoló, így az egyes készítmények terápiás eredményességéről csak a velük végzett vizsgálatok (tanulmányok, studyk, trialek) eredményeiből következtethetünk. Ezek az eredmények pedig a törzskönyvezés alapját képezik. Mindebből az is következik, hogy azoknak a kórképeknek a kezelése során, amelyekben a béta-blokkoló adása javasolt az alkalmazni kívánt készítmény kiválasztásánál – a törzskönyvezés megszabta szabályokon kívül –, számos egyéb szempontot is figyelembe érdemes venni. Egy adott indikációs körben alkalmazható két béta-blokkoló közül a járulékos tulajdonságaikat tekintve kedvezőbbet célszerű adni (lásd pl. az előbbiekben említett metabolikus hatásokat) (2. táblázat).
A diabéteszes betegek kezelésével összefüggésben érdemes néhány szót ejteni a diuretikus terápiáról is. A cukorbetegek között ugyanis gyakran találunk olyanokat, akiknél kimutatható az ún. metabolikus szindróma klinikai tünetegyüttese. Erre pedig a következő klinikai kép jellemző: hasra lokalizált, ún. abdominális elhízás, 2-es típusú cukorbetegség (pontosabban szénhidrát-háztartási zavar), hipertónia, vérzsíreltérések (alacsony HDL-koleszterin- és magas trigliceridszint), magas húgysavszint, s mindezek mellett gyakori az alvási apnoe-szindróma. Ezeknél a betegeknél tehát nagyon gyakran kényszerülünk antihipertenzív terápia beállítására. A jelenleg érvényben lévő ún. hipertóniaajánlások pedig a diuretikumokat az elsők között javasolt vérnyomáscsökkentő szerként említik. Tudni kell azonban azt, hogy a gyakran alkalmazott tiazid diuretikumok (s ezek közé tartozik a hidroklorotiazid) azokat a metabolikus paramétereket, amelyek a szervezet zsír- és szénhidrátháztartását jellemzik kedvezőtlenül befolyásolják. Ugyanakkor a szintén a diuretikumok csoportjába tartozó – tiazidszerűnek nevezett – indapamid és klórtalidon az anyagcsere-folyamatokat illetően neutrálisnak mondható. Éppen ezért számos szakmai grémium az antihipertenzív célból alkalmazni kívánt diuretikumok közül a tiazidszerűeket javasolja.
Összefoglalva elmondható, hogy a diabéteszes betegek körében gyakran megfigyelhető szív- és érrendszeri szövődmények kialakulása elkerülhető, de legalábbis lassítható. Ehhez a szénhidrátháztartás normalizálása mellett olyan gyógyszerkészítmények is a rendelkezésünkre állnak, amelyek az érelmeszesedést lassító képességekkel rendelkeznek. Ezek közül mindenképpen kiemelésre méltóak az ACE-gátlók és a DHP Ca-antagonisták. Alkalmazásukkal élni kell, ezzel is elősegítve a minél hosszabb távú, szövődménymentes túlélést.
A cikk megjelenését az Egis Gyógyszergyár Zrt. támogatta. A cikkben szereplő információk a szerző nézeteit tükrözik. Bármely említett termék alkalmazásakor az érvényes alkalmazási előírás az irányadó.
2. Microalbuminuria, Cardiovascular and Renal Outcomes in the Heart Outcomes Prevention Evaluation (Micro-HOPE Study). Lancet 2000; 355: 253–259.
3. Study to Evaluate Carotid Ultrasound changes in patients treated with Ramipril and vitamin E (Secure Study). Circulation 2001; 103: 919–925.
4. Prospective Randomized Evaluation of the Vascular Effects of Norvasc Trial. Circulation (Prevent Trial) 2000; 102: 1503– 1510.
5. Tomcsányi J. A Ramipril és Amlodipin kombináció vérnyomáscsökkentő hatékonyságának Monitorizálása és beavatkozással Nem járó Adatgyűjtése. A RAMONA vizsgálat. Hypertonia és Nephrologiai 2013; 17(2): 71–74.
6. Tomcsányi J, Simonyi G. Ramipril és Amlodipin fix kombináció vérnyomás-csökkentő hatásosságának értékelése Metabolikus Szindrómában – beavatkozással nem járó adatgyűjtés. A RAMSES vizsgálat. Hypertonia és Nephrologia. 2015; 19(1):18–24.
7. Carvedilol Or Metoprolol European Trial. (COMET Study). Lancet 2003; 362: 7–13.
8. Williams B, Mancia G. 2018 ESC/ESH Guidelines for the management of arterial hypertension. The ask Force for the management of arterial hypertension of the European Society of Cardiology (ESC) and the European Society of Hypertension (ESH). European Heart Journal 2018; 1–98.
Cikk értékelése
| Eddig 1 felhasználó értékelte a cikket. |


Hozzászólások